Чем отмыть этиленгликоль
#1 10.10.2013 11:51:31
разорвало радиатор печки на Калине Все жирное и ничего не берет. Сильно едкими веществами не пробовали, жалко пластик может кто что посоветует? #2 10.10.2013 12:21:09
для хорошо растворимого в воде вещества трудно ожидать других рекомендаций :) #3 10.10.2013 13:12:34
олежек1288, В качестве "попробовать" можно взять "растворитель монтажной пены", ну или как-то так называется (промывка для пистолета). Стирал краску с пластика. На раз-два все удалил, а пластик цел. #4 10.10.2013 13:15:32
Для того чтобы смыть немножко, то и надо немножко. А тут надо тупо вымыть весь салон: сидения, панели дверей, коврик, шумку (с той вообще беда, хоть меняй), торпеду ... #5 10.10.2013 13:29:09
Фэри вам в помощь :) #6 10.10.2013 13:29:55
силит бэнг от пятен и плесени... едкая хрень... всё чистит :) Пум пурум #7 10.10.2013 13:30:15
Антифриз смываю водой без проблем. 1 человек сказал cпасибо: (1): #8 10.10.2013 13:31:17
что тоже в салон хлещет? Пум пурум #9 10.10.2013 13:55:44
Эта гадость вообще-то только на ощупь жирная. Никакими растворителями для жира не берётся. Только вода. Раз уж , то кто мешает ковры на мойке хорошо прополоскать. Да и шумку так-же можно, только сушить потом долго. Остальное мокрой, а затем сухой тряпкой. Муторно, конечно. Я на классике так делал. Конечно не все 8 литров, но передний пассажир хорошо плавал. #10 10.10.2013 14:13:42
ну пока мы только водой и пробуем, но такое впечатление что ничего не смывает Страница 1 из 1 1 чел. читают эту тему (пользователей: 0, гостей: 1) |
|
Чем отмыть от этиленгликоля
Изобретение относится к выделению водных растворов гликолей, в частности, к способу очистки 40-90%-ных растворов гликолей отработанных антифризов, используемых для охлаждения двигателей внутреннего сгорания.
Известен способ регенерации рабочей жидкости из смеси вода-гликоль путем фильтрации и пропускания через комплексообразующую ионообменную смолу (JP заявка 62-23040, кл. С 10 М 175/04, 1987).
Известен способ получения этиленгликоля из отработанного антифризного раствора, проводимый на первой стадии на мембранах обратного осмоса, на второй стадии — пропусканием через ионообменные смолы (JP заявка 7-108141, кл. В 01 D 61/02, 1995).
Известен способ регенерации гликоля путем ректификации на колоннах при температуре 160-220oС и давлении 100-350 мм рт.ст. (SU авторское свидетельство 816099, МПК С 07 С 31/20, 1994).
Известен способ получения раствора этиленгликоля из отработанных антифризов на ионообменных мембранах в трехкамерном электродиализаторе (RU патент 2109556, кл.6 В 01 D 61/44, 1998).
Известен способ выделения этиленгликолей высокой степени чистоты путем упаривания водного раствора этиленгликолей с последующим подщелачиванием этого раствора и дистилляцией при пониженном давлении (JP патент 224399, МПК С 07 С 31/20, 1968).
Указанные способы трудоемки, требуют больших энергозатрат, хотя дают возможность получения растворов этиленгликолей достаточно высокой степени очистки, что не является обязательным условием для приготовления антифризов и низкозамерзающих теплоносителей. Для приготовления этих охлаждающих жидкостей достаточно получать водно-гликолевый раствор, очищенный от продуктов окисления этиленгликоля и продуктов коррозии, образовавшихся в процессе эксплуатации антифриза.
Наиболее близким к предлагаемому способу регенерации растворов этиленгликолей является способ очистки растворов гликолей с помощью введения коагулянта с последующим пропусканием полученной смеси через песчаный фильтр и адсорбер (SU авторское свидетельство 1685910, С 07 С 31/20, 1991). Очистка растворов гликолей достигается введением в раствор гликоля коагулянта при следующем соотношении компонентов, мас.%:
Коагулянт — 0,05-0,1
Гликоль — 50-99
Вода — Остальное
В качестве коагулянта используют фосфорнокислый натрий однозамещенный или кальцинированную соду в виде 0,1-1%-ного раствора в гликоле или воде.
Способ очистки водных растворов этиленгликоля, используемых в системах оборотного водоснабжения при охлаждении компрессоров, согласно прототипу дает неплохие результаты в случае очистки однотипных веществ. Однако из отработанного антифриза в зависимости от рецептуры должны извлекаться вещества, обладающие различными физическими и химическими свойствами, поэтому такой способ очистки нельзя считать универсальным. Его использование приводит к неполной и некачественной очистке.
Предлагаемый способ регенерации водных растворов этиленгликоля из отработанных антифризов, используемых для охлаждения двигателей внутреннего сгорания, позволяет очистить отработанный антифриз на основе гликолей от присадок, продуктов окисления и коррозии.
Целью изобретения является повышение чистоты целевого продукта и снижение энергоемкости процесса.
Поставленная цель достигается способом очистки отработанного антифриза путем его обработки гидроксидом щелочного металла, 75%-ной ортофосфорной кислоты, полифосфатом натрия, центрифугированием полученной суспензии на сепараторе (для удаления механических примесей и образовавшегося осадка продуктов коррозии и присадок за счет действия коагулянтов) и последующим пропусканием через адсорбер, заполненный активированным углем (для удаления продуктов окисления этиленгликоля), при следующем соотношении компонентов, мас.%:
Гидроксид натрия или калия — 0,01-1,0
Ортофосфорная кислота, 75%-ная — 0,02-1,6
Полифосфат натрия — 0,01-1,5
Гликоли — 40,0-90,0
Вода, продукты окисления и коррозии — Остальное
При этом в качестве полифосфата натрия используют полифосфат натрия общей формулы (NaPO3)3h3O (ГОСТ 20291-80).
Сопоставительный анализ с прототипом показывает, что коагулянт, используемый для очистки отработанного антифриза, отличается от известного введением трех новых компонентов: гидроксида щелочного металла, ортофосфорной кислоты и полифосфата натрия, а для удаления механических примесей и образовавшегося осадка используется сепаратор.
Таким образом, заявленное техническое решение соответствует критерию новизна.
Применение в данном способе очистки отработанного антифриза новых компонентов в качестве коагулянта и найденное соотношение всех ингредиентов обеспечивают максимальную степень очистки отработанного антифриза от механических примесей до 100%, продуктов окисления этиленгликоля и продуктов коррозии, образовавшихся в процессе эксплуатации антифриза, до 95,0-98,0%.
Пример 1. В емкость, снабженную мешалкой или насосом, помещают 1000 л отработанного антифриза, собранного на станции технического обслуживания, при перемешивании, при температуре окружающей среды загружают 0,1 кг гидроксида натрия, 0,2 кг 75%-ной ортофосфорной кислоты и 0,1 кг полифосфата натрия. Смесь перемешивают до растворения компонентов, оставляют на 2-3 часа для образования гелеобразного осадка (коагеля), вызванного процессом коагуляции. Полученную суспензию центрифугируют на сепараторе, и осветленную прозрачную жидкость (фугат) пропускают через адсорбер, заполненный активированным углем, со скоростью 300 л/час.
Степень очистки водно-гликолевых растворов контролируют по содержанию механических примесей, по содержанию гликолей, воды и антикоррозионных присадок, присутствующих в отработанном антифризе.
Пример 2. Очистку 1000 л отработанного антифриза проводят так же, как и в примере 1, но коагулянт содержит 5 кг гидроксида натрия, 8 кг 75%-ной ортофосфорной кислоты и 8 кг полифосфата натрия.
Пример 3. Очистку 1000 л отработанного антифриза проводят так же, как и в примере 1, но коагулянт содержит 10 кг гидроксида натрия, 16 кг 75%-ной ортофосфорной кислоты и 15 кг полифосфата натрия.
Составы коагулянтов по примерам 1-9 и прототипу представлены в таблице 1.
Степень очистки водного раствора гликолей в отработанных антифризах представлена в таблице 2.
Определение массовой доли воды, моно-, ди- и триэтиленгликолей проводят с помощью газохроматографического метода (метод внутренней нормализации) на хроматографе серии «Цвет-500», ЛХМ-8 мд или аналогичном приборе с детектором по теплопроводности. В качестве насадки для хроматографической колонки используют полисорб 1.
Уменьшение концентрации гидроксида натрия или калия ниже 0,01 мас.% не вызывает коагуляции и образования осадка в отработанном антифризе из-за недостаточного количества коагулянта (пример 4), а увеличение его выше 1,0 мас.% не приводит к повышению положительного эффекта (пример 5).
Уменьшение содержания ортофосфорной кислоты в составе коагулянта ниже 0,02 мас. % значительно снижает количество осадка в отработанном антифризе (пример 6), увеличение ее концентрации выше 1,6 мас.% приводит к снижению рН среды, что отрицательно сказывается на образовании осадка продуктов окисления этиленгликоля и продуктов коррозии (пример 7).
Снижение концентрации полифосфата натрия в составе коагулянта ниже 0,01 мас.% значительно сказывается на образовании осадка, что влечет к недостаточной очистке отработанного антифриза (пример 8), увеличение его концентрации выше 1,5 мас.% не влияет положительно на очистку (пример 9).
При соблюдении указанных значений процесса коагуляции отработанного антифриза регенерированный водный раствор этиленгликоля к концу очистки практически не содержит каких-либо примесей. Незначительные количества присадок, остающихся после очистки, играют только положительную роль в качестве дополнительного набора ингибиторов коррозии при приготовлении охлаждающих жидкостей или теплоносителя на основе регенерированного отработанного антифриза.
Основные физико-химические свойства охлаждающей жидкости, полученной на основе очищенного отработанного антифриза при дополнительном введении необходимых количеств антикоррозионных, стабилизирующих присадок и моноэтиленгликоля, представлены в таблице 3.
Таким образом, предлагаемый способ очистки отработанного антифриза позволяет получать достаточно чистый водно-гликолевый раствор, лишенный продуктов окисления этиленгликоля и продуктов коррозии, образовавшихся в процессе эксплуатации антифриза.
На основе регенерированного таким способом антифриза можно получать высококачественные охлаждающие жидкости, используемые для охлаждения двигателей внутреннего сгорания и в качестве теплоносителей. В связи с этим решается вопрос о защите окружающей среды, поскольку до сих пор неясно, куда сливать отработанные антифризы и тосол. Применение предлагаемого способа очистки отработанного антифриза позволит экономить значительные количества дорогостоящего этиленгликоля, используемого в составе охлаждающих жидкостей и теплоносителей.
ФОРМУЛА ИЗОБРЕТЕНИЯ
Способ очистки отработанного антифриза на основе водно-этиленгликолевого раствора от продуктов окисления этиленгликоля, продуктов коррозии и механических примесей, включающий добавление коагулянта и очистку на активированном угле, отличающийся тем, что в отработанный антифриз добавляют в качестве коагулянта продуктов окисления и коррозии гидроксид щелочного металла, 75%-ную ортофосфорную кислоту и полифосфат натрия при следующем соотношении компонентов, мас.%:
Гидроксид натрия или калия 0,01-1,0
Ортофосфорная кислота, 75%-ная 0,02-1,6
Полифосфат натрия 0,01-1,5
Гликоли 40,0-90,0
Вода, продукты окисления и коррозии Остальное
затем подвергают центрифугированию на сепараторе и очистке.
способ очистки отработанного антифриза на основе водно- этиленгликолевого раствора от продуктов окисления этиленгликоля, продуктов коррозии и механических примесей - патент РФ 2221766
Изобретение относится к способу очистки отработанного антифриза на основе водно-этиленгликолевого раствора, используемого для охлаждения двигателей внутреннего сгорания, от продуктов окисления этиленгликоля, продуктов коррозии и механических примесей. Способ включает добавление коагулянта и очистку на активированном угле. При этом в отработанный антифриз добавляют в качестве коагулянта продуктов окисления и коррозии гидроксид щелочного металла, 75%-ную ортофосфорную кислоту и полифосфат натрия при следующем соотношении компонентов, мас.%:Гидроксид натрия или калия - 0,01-1,0
Ортофосфорная кислота, 75%-ная - 0,02-1,6
Полифосфат натрия - 0,01-1,5
Гликоли - 40,0-90,0
Вода, продукты окисления и коррозии - Остальное
затем подвергают центрифугированию на сепараторе и очистке. Способ позволяет получать достаточно чистый водно-гликолевый раствор и снизить энергоемкость процесса. 3 табл. Рисунок 1, Рисунок 2, Рисунок 3
Формула изобретения
Способ очистки отработанного антифриза на основе водно-этиленгликолевого раствора от продуктов окисления этиленгликоля, продуктов коррозии и механических примесей, включающий добавление коагулянта и очистку на активированном угле, отличающийся тем, что в отработанный антифриз добавляют в качестве коагулянта продуктов окисления и коррозии гидроксид щелочного металла, 75%-ную ортофосфорную кислоту и полифосфат натрия при следующем соотношении компонентов, мас.%:Гидроксид натрия или калия 0,01-1,0Ортофосфорная кислота, 75%-ная 0,02-1,6Полифосфат натрия 0,01-1,5Гликоли 40,0-90,0Вода, продукты окисления и коррозии Остальноезатем подвергают центрифугированию на сепараторе и очистке.Описание изобретения к патенту
Изобретение относится к выделению водных растворов гликолей, в частности, к способу очистки 40-90%-ных растворов гликолей отработанных антифризов, используемых для охлаждения двигателей внутреннего сгорания. Известен способ регенерации рабочей жидкости из смеси вода-гликоль путем фильтрации и пропускания через комплексообразующую ионообменную смолу (JP заявка 62-23040, кл. С 10 М 175/04, 1987). Известен способ получения этиленгликоля из отработанного антифризного раствора, проводимый на первой стадии на мембранах обратного осмоса, на второй стадии - пропусканием через ионообменные смолы (JP заявка 7-108141, кл. В 01 D 61/02, 1995). Известен способ регенерации гликоля путем ректификации на колоннах при температуре 160-220oС и давлении 100-350 мм рт.ст. (SU авторское свидетельство 816099, МПК С 07 С 31/20, 1994). Известен способ получения раствора этиленгликоля из отработанных антифризов на ионообменных мембранах в трехкамерном электродиализаторе (RU патент 2109556, кл.6 В 01 D 61/44, 1998). Известен способ выделения этиленгликолей высокой степени чистоты путем упаривания водного раствора этиленгликолей с последующим подщелачиванием этого раствора и дистилляцией при пониженном давлении (JP патент 224399, МПК С 07 С 31/20, 1968). Указанные способы трудоемки, требуют больших энергозатрат, хотя дают возможность получения растворов этиленгликолей достаточно высокой степени очистки, что не является обязательным условием для приготовления антифризов и низкозамерзающих теплоносителей. Для приготовления этих охлаждающих жидкостей достаточно получать водно-гликолевый раствор, очищенный от продуктов окисления этиленгликоля и продуктов коррозии, образовавшихся в процессе эксплуатации антифриза. Наиболее близким к предлагаемому способу регенерации растворов этиленгликолей является способ очистки растворов гликолей с помощью введения коагулянта с последующим пропусканием полученной смеси через песчаный фильтр и адсорбер (SU авторское свидетельство 1685910, С 07 С 31/20, 1991). Очистка растворов гликолей достигается введением в раствор гликоля коагулянта при следующем соотношении компонентов, мас.%:Коагулянт - 0,05-0,1
Гликоль - 50-99
Вода - Остальное
В качестве коагулянта используют фосфорнокислый натрий однозамещенный или кальцинированную соду в виде 0,1-1%-ного раствора в гликоле или воде. Способ очистки водных растворов этиленгликоля, используемых в системах оборотного водоснабжения при охлаждении компрессоров, согласно прототипу дает неплохие результаты в случае очистки однотипных веществ. Однако из отработанного антифриза в зависимости от рецептуры должны извлекаться вещества, обладающие различными физическими и химическими свойствами, поэтому такой способ очистки нельзя считать универсальным. Его использование приводит к неполной и некачественной очистке. Предлагаемый способ регенерации водных растворов этиленгликоля из отработанных антифризов, используемых для охлаждения двигателей внутреннего сгорания, позволяет очистить отработанный антифриз на основе гликолей от присадок, продуктов окисления и коррозии. Целью изобретения является повышение чистоты целевого продукта и снижение энергоемкости процесса. Поставленная цель достигается способом очистки отработанного антифриза путем его обработки гидроксидом щелочного металла, 75%-ной ортофосфорной кислоты, полифосфатом натрия, центрифугированием полученной суспензии на сепараторе (для удаления механических примесей и образовавшегося осадка продуктов коррозии и присадок за счет действия коагулянтов) и последующим пропусканием через адсорбер, заполненный активированным углем (для удаления продуктов окисления этиленгликоля), при следующем соотношении компонентов, мас.%:
Гидроксид натрия или калия - 0,01-1,0
Ортофосфорная кислота, 75%-ная - 0,02-1,6
Полифосфат натрия - 0,01-1,5
Гликоли - 40,0-90,0
Вода, продукты окисления и коррозии - Остальное
При этом в качестве полифосфата натрия используют полифосфат натрия общей формулы (NaPO3)3H2O (ГОСТ 20291-80). Сопоставительный анализ с прототипом показывает, что коагулянт, используемый для очистки отработанного антифриза, отличается от известного введением трех новых компонентов: гидроксида щелочного металла, ортофосфорной кислоты и полифосфата натрия, а для удаления механических примесей и образовавшегося осадка используется сепаратор. Таким образом, заявленное техническое решение соответствует критерию новизна. Применение в данном способе очистки отработанного антифриза новых компонентов в качестве коагулянта и найденное соотношение всех ингредиентов обеспечивают максимальную степень очистки отработанного антифриза от механических примесей до 100%, продуктов окисления этиленгликоля и продуктов коррозии, образовавшихся в процессе эксплуатации антифриза, до 95,0-98,0%. Пример 1. В емкость, снабженную мешалкой или насосом, помещают 1000 л отработанного антифриза, собранного на станции технического обслуживания, при перемешивании, при температуре окружающей среды загружают 0,1 кг гидроксида натрия, 0,2 кг 75%-ной ортофосфорной кислоты и 0,1 кг полифосфата натрия. Смесь перемешивают до растворения компонентов, оставляют на 2-3 часа для образования гелеобразного осадка (коагеля), вызванного процессом коагуляции. Полученную суспензию центрифугируют на сепараторе, и осветленную прозрачную жидкость (фугат) пропускают через адсорбер, заполненный активированным углем, со скоростью 300 л/час. Степень очистки водно-гликолевых растворов контролируют по содержанию механических примесей, по содержанию гликолей, воды и антикоррозионных присадок, присутствующих в отработанном антифризе. Пример 2. Очистку 1000 л отработанного антифриза проводят так же, как и в примере 1, но коагулянт содержит 5 кг гидроксида натрия, 8 кг 75%-ной ортофосфорной кислоты и 8 кг полифосфата натрия. Пример 3. Очистку 1000 л отработанного антифриза проводят так же, как и в примере 1, но коагулянт содержит 10 кг гидроксида натрия, 16 кг 75%-ной ортофосфорной кислоты и 15 кг полифосфата натрия. Составы коагулянтов по примерам 1-9 и прототипу представлены в таблице 1. Степень очистки водного раствора гликолей в отработанных антифризах представлена в таблице 2. Определение массовой доли воды, моно-, ди- и триэтиленгликолей проводят с помощью газохроматографического метода (метод внутренней нормализации) на хроматографе серии "Цвет-500", ЛХМ-8 мд или аналогичном приборе с детектором по теплопроводности. В качестве насадки для хроматографической колонки используют полисорб 1. Уменьшение концентрации гидроксида натрия или калия ниже 0,01 мас.% не вызывает коагуляции и образования осадка в отработанном антифризе из-за недостаточного количества коагулянта (пример 4), а увеличение его выше 1,0 мас.% не приводит к повышению положительного эффекта (пример 5). Уменьшение содержания ортофосфорной кислоты в составе коагулянта ниже 0,02 мас. % значительно снижает количество осадка в отработанном антифризе (пример 6), увеличение ее концентрации выше 1,6 мас.% приводит к снижению рН среды, что отрицательно сказывается на образовании осадка продуктов окисления этиленгликоля и продуктов коррозии (пример 7). Снижение концентрации полифосфата натрия в составе коагулянта ниже 0,01 мас.% значительно сказывается на образовании осадка, что влечет к недостаточной очистке отработанного антифриза (пример 8), увеличение его концентрации выше 1,5 мас.% не влияет положительно на очистку (пример 9). При соблюдении указанных значений процесса коагуляции отработанного антифриза регенерированный водный раствор этиленгликоля к концу очистки практически не содержит каких-либо примесей. Незначительные количества присадок, остающихся после очистки, играют только положительную роль в качестве дополнительного набора ингибиторов коррозии при приготовлении охлаждающих жидкостей или теплоносителя на основе регенерированного отработанного антифриза. Основные физико-химические свойства охлаждающей жидкости, полученной на основе очищенного отработанного антифриза при дополнительном введении необходимых количеств антикоррозионных, стабилизирующих присадок и моноэтиленгликоля, представлены в таблице 3. Таким образом, предлагаемый способ очистки отработанного антифриза позволяет получать достаточно чистый водно-гликолевый раствор, лишенный продуктов окисления этиленгликоля и продуктов коррозии, образовавшихся в процессе эксплуатации антифриза. На основе регенерированного таким способом антифриза можно получать высококачественные охлаждающие жидкости, используемые для охлаждения двигателей внутреннего сгорания и в качестве теплоносителей. В связи с этим решается вопрос о защите окружающей среды, поскольку до сих пор неясно, куда сливать отработанные антифризы и тосол. Применение предлагаемого способа очистки отработанного антифриза позволит экономить значительные количества дорогостоящего этиленгликоля, используемого в составе охлаждающих жидкостей и теплоносителей.
Этиленгликоль чем отмыть бочку
Êàæäûé âèíîäåë è âèíîêóð (äà è ëþáàÿ äîìîõîçÿéêà òîæå) íåèçìåííî ñòàëêèâàåòñÿ ñ ìûòüåì åìêîñòåé, è îò êà÷åñòâà î÷èñòêè ÷àñòåíüêî çàâèñèò è ñóäüáà áóäóùåãî ïðîäóêòà.
Âîçüìåì, ê ïðèìåðó, ïðîèçâîäñòâî âèíà, — äåëî òîíêîå è òðåáóþùåå ñòåðèëüíîñòè. Ñïîëîñíóëè äâàäöàòèëèòðîâóþ áóòûëü àáû-êàê, çàëèëè â íåå ñâåæåâûæàòûé ñîê, à âìåñòî îæèäàåìîãî «íåêòàðà» ïîëó÷èëè óêñóñ. Åùå õóæå åñëè çàëèâàåòå âêóñíîå âèíî, ñòàâèòå â ïîãðåá, à îíî ïðîêèñàåò.
À âñå äåëî â òîì, ÷òî åìêîñòü íåêà÷åñòâåííî âûìûòà. ß äàâíî ïîíÿë, ÷òî ýòîìó âîïðîñó î÷èñòêè åìêîñòåé íàäî óäåëÿòü ïîâûøåííîå âíèìàíèå. Ðàññêàæó, ïðî êàêèå ñïîñîáû ÿ íàøåë èíôîðìàöèþ è â êîíöå ñòàòüè ïî÷åìó ÷èñòîòà òàðû êðàéíå âàæíà â äîìàøíåì ñàìîãîíîâàðåíèè.
Ïîìåíüøå õèìèè
Åñòåñòâåííî, áûñòðåå âñåãî ñ çàãðÿçíåíèÿìè ñïðàâèòñÿ õèìèÿ, íî íàäî ëè åå ïðèìåíÿòü ê òîìó, ÷òî áóäåò ñîïðèêàñàòüñÿ ñ åäîé è íàïèòêàìè? Çíà÷èòåëüíî áåçîïàñíåå ïðèìåíÿòü íàòóðàëüíûå ñðåäñòâà, òîëüêî â ñàìîì êðàéíåì ñëó÷àå îáðàùàÿñü ê õèìè÷åñêèì âåùåñòâàì.
Íàðîäíûå ñïîñîáû
Ðàññìîòðèì íåîäíîêðàòíî ïðîâåðåííûå è çàñëóæèâàþùèå äîâåðèÿ ñïîñîáû, ñ ïîìîùüþ êîòîðûõ ìîæíî îòìûòü èçíóòðè äàæå î÷åíü «çàïóùåííûå» çàãðÿçíåíèÿ:
1. ßè÷íàÿ ñêîðëóïà è ïèùåâàÿ ñîäà. Ýòîò òàíäåì ïðèãîäèòñÿ, ÷òîáû êà÷åñòâåííî âûìûòü ñîñóä, îñîáåííî òîò, â êîòîðûé íå ïðîñóíåøü ðóêó èëè íå äîñòàíåøü äî äíà. Òàêîé, êàê áóòûëü äëÿ âèíà èëè áóòûëêà. Ïîíàäîáèòñÿ:
ÿè÷íàÿ ñêîðëóïà îò íåñêîëüêèõ ÿèö. Ìîæíî áðàòü êàê îò âàðåíûõ, òàê è îò ñûðûõ. Ãëàâíîå èçìåëü÷èòü (ðàçìÿòü) åå ðóêàìè äî ìåëêèõ êóñî÷êîâ, íå áîëåå 0,5 ñì;
ïèùåâàÿ ñîäà èç ðàñ÷åòà 50 ã íà ëèòð âîäû;
òåïëàÿ âîäà. Ýòî îáÿçàòåëüíîå óñëîâèå, ÷òîáû çàãðÿçíåíèÿ îò÷èñòèëèñü.
Èòàê, ðàñòâîðèòå ñîäó â òåïëîé âîäå. Âîçìîæíî, âîäû ïîíàäîáèòñÿ áîëüøå, åñëè åìêîñòü áîëüøàÿ.  òàêîì ñëó÷àå äîáàâüòå è ñîäû ïðîïîðöèîíàëüíî. Íà 20-ëèòðîâóþ áóòûëü íóæíî 3-5 ëèòðîâ ðàñòâîðà è ñêîðëóïà 5-6 ÿèö. Çàñûïüòå èçìåëü÷åííóþ ñêîðëóïó, âëåéòå ñîäîâûé ðàñòâîð. Ñëåãêà âçáîëòàéòå åìêîñòü, ÷òîáû ñìî÷èòü çàãðÿçíåííûå ìåñòà.
Îñòàâüòå òàê íà ïàðó ÷àñîâ. Ïîñëå ÷åãî òðÿñèòå ýíåðãè÷íî ìèíóò 10. Óñòàíåòå, ïåðåäîõíèòå è ñíîâà òðÿñèòå. Âûìûòóþ åìêîñòü íåñêîëüêî ðàç ñïîëîñíèòå ÷èñòîé âîäîé. Âàæíî âûìûòü âñå îñòàòêè ñêîðëóïû.
Ñïîñîá, îïèñàííûé âûøå ïîäõîäèò äëÿ âñåõ âèäîâ ïîñóäû: îò ñòåêëà äî ïëàñòèêà.
2. Îáû÷íûì ïøåíîì. Îíî íåïëîõî ñïðàâëÿåòñÿ ñ íàëåòîì âíóòðè åìêîñòåé. Çàñûïüòå â áóòûëü îáû÷íîå ïøåíî (ïðèìåðíî ïîëîâèíà ïà÷êè íà 20-25-ëèòðîâóþ áóòûëü). Çàëåéòå íåñêîëüêî ëèòðîâ âîäû, ìîæíî õîëîäíîé. È òðÿñèòå-òðÿñèòå, ïîêà âíóòðåííÿÿ ïîâåðõíîñòü íå î÷èñòèòñÿ. Åùå ëó÷øå çàñåêèòå 10 ìèíóò. Ñïîëîñíèòå âàøó ïîñóäèíó.
3. Ñòàðûìè ãàçåòàìè. Êñòàòè, çàìå÷åíî, ÷òî ëó÷øå ðàáîòàþò èìåííî ãàçåòû, à íå ÷èñòàÿ áóìàãà. Ìîæåò, â òèïîãðàôñêîé êðàñêå òàêæå åñòü êàêîé-òî êîìïîíåíò, êîòîðûé ïîìîãàåò ñïðàâèòüñÿ ñ ãðÿçüþ è íàëåòîì. Ýòî è ñ îáû÷íûìè îêîííûìè ñòåêëàìè ðàáîòàåò. ×òîáû áóòûëü ñòàë ÷èñòûì, ïîðâèòå ãàçåòó è íàäåëàéòå èç íåå øàðèêîâ. Ïîáðîñàéòå â åìêîñòü, çàëåéòå âîäîé è ñ ýíòóçèàçìîì òðÿñèòå. Åñëè èìååòå äåëî ñî ñòåêëîì, òî óâèäèòå ñòåïåíü î÷èñòêè, åñëè ó âàñ, ê ïðèìåðó, ìåòàëëè÷åñêàÿ èëè ïëàñòèêîâàÿ êàíèñòðà, ëó÷øå âûäåëèòå äëÿ ýòîãî çàíÿòèÿ 10 ìèíóò.
4. Êðàïèâà ñ ñîäîé â òåïëîé âîäå. È ñîäà, è êðàïèâà ïîìèìî î÷èùàþùèõ ñïîñîáíîñòåé, èìåþò åùå è äåçèíôèöèðóþùèå, ÷òî îñîáåííî âàæíî, åñëè â ðåçåðâóàðå åñòü ïëåñåíü èëè îñòàòêè çåëåíè íà ñòåíêàõ. Ëó÷øå âñåãî íàðâàòü êðàïèâû íà áëèæíåì ïóñòûðå è íàòîëêàòü åå â áàê èëè áóòûëü, íå çàáûâàÿ çàùèùàòü ðóêè, ïîñêîëüêó ýòà òðàâà ñèëüíî æàëèòñÿ. Íåêîòîðûå èñïîëüçóþò ñóõóþ, èç àïòåêè. Êàê ãîòîâèòü ðàñòâîð ñîäû â òåïëîé âîäå, âû óæå çíàåòå. Äàéòå ïîñòîÿòü ÷àñîê-äðóãîé, è çàòåì ìåõàíè÷åñêèì ñïîñîáîì (èíòåíñèâíûì âñòðÿõèâàíèåì) âûìîéòå âíóòðåííþþ ÷àñòü áóòûëè èëè êàíèñòðû.
5. Ïåðåêèñü âîäîðîäà. Íå ïðîñòî ñèëüíûé àíòèñåïòèê, íî åùå è ïðåêðàñíîå îòáåëèâàþùåå ñðåäñòâî. Îñîáåííî õîðîøî äåéñòâóåò â òàíäåìå ñ ñîäîé.  áóòûëêó çàñûïüòå ïîë ïà÷êè ïèùåâîé ñîäû è âëåéòå ôëàêîí÷èê àïòå÷íîé ïåðåêèñè (100 ìë). Íåìåäëåííî òðÿñèòå, ðàñïðåäåëÿÿ ïîëó÷åííóþ ñìåñü âíóòðè. Ïîäîæäèòå ñ ïîë ÷àñà, äîëåéòå òåïëîé âîäû è åùå õîðîøåíüêî ïîòðÿñèòå. Òåïåðü ùåäðî îïîëàñêèâàéòå âîäîé. Ïåðåêèñü íàïðî÷ü óíè÷òîæàåò ëþáûå âèðóñû, ãðèáêè, áàêòåðèè, ïîýòîìó îñîáåííî ïîäõîäèò äëÿ «ïîäîçðèòåëüíîé» ïîñóäû, íàïðèìåð ñòàðèííûõ áóòûëîê.
×èñòêà è ìûòüå äðóãèìè ñïîñîáàìè
Êðîìå îïèñàííûõ, ìîæíî èñïîëüçîâàòü è äðóãèå «ïîäðó÷íûå» ïðèñïîñîáëåíèÿ, ÷òîáû äîâåñòè âíóòðåííþþ ÷àñòü åìêîñòåé äî âûñîêîé ñòåïåíè ÷èñòîòû:
Ñòàðîå ïîëîòåíöå, êîòîðîãî óæå íå æàëêî, ëó÷øå ïîðâàòü íà ïîëîñû è èñïîëüçîâàòü âìåñòî áóìàãè.
Ìîþùèå ñðåäñòâà ìîæíî èñïîëüçîâàòü â ñî÷åòàíèè ñ ïåñêîì, êðóïîé è ò.ï.
«Áåëèçíà» õîðîøî ñïðàâëÿåòñÿ ñ çåëåíüþ, íàëåòîì, ïÿòíàìè îò âèíà. Íî ó íåå åñòü è íåãàòèâíûé ìîìåíò: õëîðíûé çàïàõ, êîòîðûé ïî÷òè íåèñòðåáèì íà äåðåâå èëè ïëàñòèêå. À âîò ñòåêëî è êåðàìèêó ñ åå ïîìîùüþ ìîæíî ïðåêðàñíî îòìûòü. Çàòåì ìíîãî ðàç ñïîëîñíóòü è äàòü ïîñòîÿòü îòêðûòûì, ÷òîáû çàïàõ âûâåòðèëñÿ.
Äðåâåñíàÿ ñòðóæêà åùå îäíî íåïëîõîå ìåõàíè÷åñêîå ñðåäñòâî. Èì ìîæíî ÷èñòèòü ïî÷òè âñå, âêëþ÷àÿ äåðåâÿííûå áî÷êè.
Êàðòîôåëüíûå î÷èñòêè ÷èñòÿò íå òîëüêî áëàãîäàðÿ «èñòèðàíèþ» ïîâåðõíîñòè, íî è ñîäåðæàùåìóñÿ â íèõ êðàõìàëó.
Êðóïû è çåðíî. Êðîìå óæå íàçâàííîãî ïøåíà ïðåêðàñíî çàðåêîìåíäîâàë ñåáÿ ðèñ. À âîò ãðå÷êó ìíîãèå íå ðåêîìåíäóþò èñïîëüçîâàòü, ïîñêîëüêó îíà áûñòðî âïèòûâàåò âîäó, ñòàíîâèòñÿ ðûõëîé è ïëîõî âûìûâàåòñÿ. Ìîæíî èñïîëüçîâàòü öåëüíîå çåðíî: ïøåíèöó, îâåñ, ðîæü.
Ïåñîê è íàòåðòîå íà òåðêå õîçÿéñòâåííîå ìûëî èçáàâÿò åìêîñòü äàæå îò æèðíîãî íàëåòà.
Ãîð÷è÷íûé ïîðîøîê è òåïëàÿ âîäà (áëèæå ê ãîðÿ÷åé) îòìûâàþò áîëüøèíñòâî çàãðÿçíåíèé, âêëþ÷àÿ ìàñëî.
Óêñóñ èëè ëèìîííàÿ êèñëîòà ïðåêðàñíîå ñðåäñòâî îò íàëåòà. Ëó÷øå ïîëíîñòüþ çàëèòü ãðÿçíûå ìåñòà è îñòàâèòü íà íî÷ü, à ïîòîì âçáîëòàòü, ñïîëîñíóòü è ïðè ïîòðåáíîñòè èñïîëüçîâàòü ñðåäñòâà äëÿ ìåõàíè÷åñêîé î÷èñòêè.
Îñòîðîæíî. Ñîåäèíÿòü õëîðêó è êèñëîòû íåëüçÿ íè â êîåì ñëó÷àå. Ëèáî òî, ëèáî äðóãîå.
Íî åñëè, ê ïðèìåðó, íå ïîìîã óêñóñ, è ñîáèðàåòåñü âîñïîëüçîâàòüñÿ «Áåëèçíîé» (âîò âàðèàíò 3 â 1), âíà÷àëå õîðîøî îïîëîñíèòå åìêîñòü îò îñòàòêîâ êèñëîòû.
Âîò òàêèå íåõèòðûå, íî äåéñòâåííûå ñïîñîáû ìûòüÿ è äåçèíôåêöèè òî÷íî ïîìîãóò, êîãäà âàì ïîíàäîáèòñÿ ÷èñòàÿ ïîñóäà äëÿ âèíà, ïîñòàíîâêè áðàãè èëè î÷èñòêà äåòàëåé ñàìîãîííîãî àïïàðàòà.
Ñòåðèëüíîñòü â âèíîäåëèè è ñàìîãîíîâàðåíèè
À âû çíàåòå, ÷òî ïðåíåáðåæåíèåì íîðì ñòåðèëüíîñòè ìîæíî ïîãóáèòü áðàãó è âèíîìàòåðèàë. Âîò íåñêîëüêî ôàêòîâ:
 ãðÿçíîé åìêîñòè äðîææåâûå ãðèáêè ìîãóò «âûòåñíèòü» óêñóñíûå èëè ïëåñíåâûå, è áðàãà íå ñîçðååò, à ñêèñíåò.
Åùå âàæíåå ÷èñòàÿ ïîñóäà è âåñü ñîïðèêàñàþùèéñÿ ñ ñóñëîì èíñòðóìåíò ïðè ïîñòàíîâêå çåðíîâîé áðàãè è â ïèâîâàðåíèè.
Âñÿ ïîñóäà äëÿ âèíà (ñóëåè, áóòûëè, áðîäèëüíûå åìêîñòè) äîëæíà áûòü ñòåðèëüíî ÷èñòîé äëÿ ïðàâèëüíîãî âèííîãî, à íå óêñóñíîãî áðîæåíèÿ.
Ìåëêèå îñòàòêè áàðäû (îòðàáîòàííîé áðàãè) â ïåðåãîííîì êóáå è äåòàëÿõ ñàìîãîííîãî àïïàðàòà ïðèâîäÿò ê èñïîð÷åííîìó äèñòèëëÿòó ñ íåïðèÿòíûì çàïàõîì è âêóñîì.
Ïîýòîìó íå çàáûâàéòå î ÷èñòîòå âñåé ïîñóäû, êîòîðóþ èñïîëüçóåòå â ñâîåì àðñåíàëå.
Íà îäíîì èçâåñòíîì ôîðóìå ñàìîãîíùèêîâ óâèäåë îáñóæäåíèå ïàðîî÷èñòèòåëÿ, êàê âàðèàíò óäàëåíèÿ çàãðÿçíåíèé â òðóäíîäîñòóïíûõ ìåñòàõ, ìíåíèÿ òàì ðàçäåëèëèñü — êòî-òî äîâîëåí, à êòî-òî íàøåë êó÷ó íåäîñòàòêîâ â ýòîì ñïîñîáå. ß ïîøåë äàëüøå è ñòàë èñêàòü îòçûâû â èíòåðíåòå è íàøåë îäèí îòçûâ ïî Êåðõåðó, êîòîðûé âïîëíå äîñòîèí Ïóëèòöåðîâñêîé ïðåìèè. )))
(ñàì îòçûâ â âèäå êàðòèíêè íèæå)
Åñëè ìàòåðèàë âàì ïîëåçåí ñòàâüòå ëàéêè è äåëèòåñü ñ äðóçüÿìè ïî ñîöñåòÿì. Äåëèòåñü îïûòîì, ìîæåò ýòî íå âñå ñïîñîáû òàêîé î÷èñòêè.
Этиленгликоль, очистка - Справочник химика 21
Получение этиленгликоля из формальдегида организовано в США фирмой Е. I. du Pont de Nemours and o. По этому способу смесь паров формальдегида и воды (объемное соотношение 1 1) абсорбируется водным раствором гликолевой кислоты (мольное соотношение 1 2) с примесью каталитических количеств серной кислоты и затем пропускается через реактор вместе с избытком окиси углерода при 200 "С и 70 МПа (время контакта 5 мин). В результате образуется гликолевая кислота (выход 90—95%), выделяемая перегонкой прн пониженном давлении. После этерификации гликолевой кислоты метиловым спиртом и очистки зфира перегонкой, проводится гидрирование метилового эфира гликолевой кислоты при 200 °С и 3 МПа в присутствии катализатора медь—хромат бария. На стадии восстановления получают этиленгликоль с выходом 90%. Данный метод не получил широкого распространения вследствие многостаднйности и высокой коррозионности среды, но может быть перспективным при снижении стоимости и расщирении производства синтез-газа. [c.274]
Чистый моновиниловый эфир этиленгликоля получают дальнейшим фракционированием продукта реакции при атмосферном давлении в присутствии поташа или в вакууме беа него. Дивиниловый эфир этиленгликоля многократно промывают водой, высушивают поташом, затем обрабатывают на холоду металлическим натрием и перегоняют в отсутствии металлического натрия. Для очистки циклического ацеталя этиленгликоля его обрабатывают на холоду металлическим натрием, а затем перегоняют над ним. [c.42]
Из ароматических полиэфиров в промышленном масштабе производится полиэтилентерефталат. Волокно из этого полимера выпускается в СССР под названием лавсан , в Англии — терилен , в США — дакрон и т. д. Исходными продуктами для синтеза полиэтилентерефталата являются терефталевая кислота и этиленгликоль. Вследствие трудности очистки терефталевой кислоты ее сначала этерифицируют метанолом, полученный диметилтерефталат переэтерифицируют этилен-гликолем (этот процесс сопровождается частичной поликонденсацией) [c.350]
Этиленгликоль получается преимущественно прямым каталитическим окислением этилена в этиленоксид с последующей ее гидратацией. Этиленоксид может быть превращен в гликоль каталитической или екаталитической гидратацией. В каталитическом процессе требуется большой избыток разбавленных водных кислот, обычно серной, а в некаталитическом — избыток воды. Реакция каталитического процесса проводится при 180°С и 21,5-105 11а, а некаталитичеокого процесса — при 95 °С и (15—20)-10 Па. Побочными продуктами реакции являются ди- и триэтиленгликоли, составляющие соответственно 9% и 1% (масс.). При этом выходы этих гликолей могут быть повышены увеличением температуры и небольшим понижением давления в реакторе. Небольшие количества полиэтиленглико-лей образуются также при обычных условиях, но выход их может быть увеличен при использовании в качестве катализатора аОН. Для разделения и очистки гликолей проводят дегидратацию реакционной смеси с последующей вакуумной перегонкой. [c.272]
Имеются указания [272, 311—314] о возможности применения азеотропной ректификации для выделения и очистки стирола. Стирол высокой степени чистоты можно получить путем азеотропной ректификации узких фракций, выделяемых из смесей, образующихся в коксовых печах при производстве водяного газа или при крекинге и риформинге нефтяных масел. В качестве разделяющих агентов могут применяться метиловый эфир этиленгликоля [272, 311—313], метиллактат, этиллактат [311], многоатомные спирты [312], а также жирные кислоты Сг—С4, особенно уксусная [314]. В процессе азеотропной ректификации стирол остается в кубе, а в виде азеотропов отгоняются более насыщенные углеводороды. Во избежание полимеризации стирола процесс проводится под вакуумом. [c.280]
В головке колонки. После окончания перегонки выключают электрический обогрев и охлаждающую воду, а также отключают вакуум. До отключения вакуума колонку целесообразно заполнить инертным газом во избежание окисления остатков вещества в колонке и перегонной колбе. После охлаждения определяют вес остатка в перегонной колбе и вес статической задержки, оставшейся в колонке, для чего колонку с перегонной колбой взвешивают до и после очистки. Если после перегонки остается высококипящий остаток, то колонку можно очистить добавкой низкокипящего растворителя (этиловый эфир, ацетон) через 1—2 час работы с полным орошением колонка и ее головка полностью отмываются. После этого содержимое перегонной колбы количественно переносят в взвешенную колбочку, отгоняют растворитель, снова взвешивают и находят таким образом общий вес кубового остатка и задержки колонки. Иногда в процессе ректификации колонка загрязняется вязкими полимерами, не растворяющимися в низкокипящих растворителях. В таких случаях для их вымывания следует использовать специальные растворители, например пиридин, монометиловый эфир эти
что такое, применение, отравление — симптомы, первая помощь, лечение, профилактика
 Один из типичных представителей спиртов — это этиленгликоль. Эта жидкость входит в состав многих химических средств в том числе для ухода за машинами и помещениями. Но так как этиленгликоль имеет непосредственное отношение к спиртам — его периодически пытаются выпить как заменитель алкоголя. Не все знают, что именно этот представитель обладает наиболее выраженными отравляющими качествами.
Один из типичных представителей спиртов — это этиленгликоль. Эта жидкость входит в состав многих химических средств в том числе для ухода за машинами и помещениями. Но так как этиленгликоль имеет непосредственное отношение к спиртам — его периодически пытаются выпить как заменитель алкоголя. Не все знают, что именно этот представитель обладает наиболее выраженными отравляющими качествами.
Что такое этиленгликоль, какая у него формула и физические свойства? Как его получают и где применяют? Чем опасен для организма человека этот спирт? В каких случаях происходит отравление им и что за симптомы беспокоят при этом? Как нужно действовать, чтобы помочь пострадавшему?
Что такое этиленгликоль
Этиленгликоль — это представитель спиртов с двумя метильными группами в своём составе. Но в отличие от других он имеет немного маслянистую консистенцию.
Несмотря на то что этиленгликоль был получен ещё в 1859 году, он не сразу занял свою нишу в химии и промышленности. Изначально он использовался во времена Первой мировой войны, как замена глицерина, который широко применялся при производстве взрывчатых веществ.
Химическая формула этиленгликоля — C2H6O2, рациональная — С2Н4(ОН)2. По своим физическим свойствам — это жидкость без запаха, но со сладким вкусом. Он легко соединяется с водой в любой консистенции, что успешно применяется в промышленности, ведь температура замерзания таких жидкостей очень низкая — это улучшает свойства «незамерзаек».
 У этиленгликоля есть несколько названий, которые нередко можно встретить в составе продуктов химического производства:
У этиленгликоля есть несколько названий, которые нередко можно встретить в составе продуктов химического производства:
- гликоль;
- этандиол-1,2;
- 1,2-диоксиэтан.
Чаще других употребляется основное название.
К какому классу опасности относится этиленгликоль? — к умеренно токсичное легковоспламеняющееся вещество.
Способы получения
Производством этиленгликоля в промышленных масштабах занялись ещё в тридцатые годы прошлого века. Одним из способов его получения тогда было окисление этилена до его оксида. Около 20 лет такой метод оставался единственным.
Немного позже этиленгликоль стали получать с помощью насыщения оксида этилена водой, в присутствии серной и ортофосфорной кислот. Этот способ оказался выгодней предыдущего, так как на выходе производили более 90% этиленгликоля с минимальным количеством примесей.
Где применяется
В основном этиленгликоль используют в промышленности для обработки техники, что обусловлено его стоимостью — это недорогой и всем доступный продукт.
 Он выпускается в химической промышленности для ухода за автомобилями:
Он выпускается в химической промышленности для ухода за автомобилями:
- более 50% вещества идёт на создание тормозных жидкостей и антифризов, так как смесь гликоля и воды способна сохранять жидкую консистенцию даже при 40º C ниже нуля;
- этиленгликоль входит в состав охлаждающей жидкости — тосола;
- он может устранять коррозию, поэтому гликоль добавляют в антикоррозийные химические соединения.
Где ещё используется этиленгликоль?
- Его можно обнаружить в составе антистатиков.
- Используют для производства средств защиты против обледенения.
- Служит смазкой в холодильных установках.
- Находит применение этиленгликоль как наполнитель в гидравлических системах.
- Гликоль нередко используют для дезинфекции больших помещений.
- Одно из ключевых применений вещества — это производство бытовых химических продуктов, к числу которых относится целлофан, полиуретан.
- Он используется не только при охлаждении автомобилей, но и компьютеров.
- Этиленгликоль или химические соединения в составе с ним применяется, как средство для чистки автомобильных стёкол и зеркал.
- В небольшом количестве присутствует в креме для обработки обуви.
- Применяется этиленгликоль и в медицине, как составная часть криопротекторов для тканей и органов. То есть веществ, которые используют для заморозки.
- Это один из компонентов конденсаторов.
- Ключевым свойством этиленгликоля является поглощение воды, что успешно используется, чтобы предотвратить обледенение топлива в авиации и синтеза гидрата метана в трубопроводах, которые проходят в море.
- В органической химии его применяют как высокотемпературный растворитель.
- Без него не проходит синтез химических соединений.
- Где ещё используется этиленгликоль? — даже в наше время с его участием создают взрывчатые вещества.
За прошедшие десятилетия для этого двухатомного спирта нашлось множество применений, что, конечно же, обусловлено его свойствами. Но в медицине он известен не только как полезный и нужный продукт в быту, но и как средство, после контакта с которым человек может умереть.
Так что это такое этиленгликоль? — полезное химическое вещество, без которого не обходится производство большинства органических соединений или сильнодействующий яд с мощным отравляющим эффектом? Давайте узнаем, как может повлиять этиленгликоль на человека.
Влияние этиленгликоля на организм человека
Этот двухатомный спирт в основном входит в состав продуктов для ухода за помещениями, машинами и техникой. По своим физическим свойствам он отличается от привычного спирта маслянистой консистенцией и отсутствием запаха, поэтому его сложно перепутать с этанолом или изопропанолом, которые нередко употребляют внутрь. Возможны ли отравления этиленгликолем у людей? — да, несмотря на явные различия с другими спиртами отравиться им можно.
В каких случаях происходит отравление?
 Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно.
Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно.- Гликоль попадает внутрь при постоянной работе с ним, к примеру, если человек трудится на химическом производстве продуктов, содержащих этиленгликоль.
- Отравиться можно при случайном употреблении его внутрь.
- Так как это химическое соединение используется для обработки машин, то в группе риска находятся люди, регулярно сталкивающиеся с ним по долгу службы.
Этиленгликоль токсичен и относится к веществам третьего класса опасности. После поступления в организм человека он очень быстро всасывается в желудке и верхнем отделе тонкого кишечника. Не более 30% его выделяется в неизменном состоянии почками или в виде солей. Остальная же часть поступает в печень, где и происходит его преобразование.
В печени он разлагается до конечных продуктов:
- гликолевой кислоты;
- муравьиной и щавелевой кислоты;
- гликолевого альдегида.

Как влияет этиленгликоль на организм человека? Все эти конечные продукты распада действуют на кислотно-щелочное равновесие, что постепенно приводит к некрозу клеток головного мозга и почечной ткани. В организме развивается ацидоз или увеличение кислотности. Смертельная доза для человека составляет всего 100–150 мл. Но даже попадание небольшого количества этиленгликоля приведёт к развитию отравления, хотя и в лёгкой степени.
Симптомы отравления
В воспалительный процесс после употребления этиленгликоля вовлекаются не только почки и головной мозг. Спирт и его конечные продукты влияют на все системы органов. Скрытый период отравления этиленгликолем в среднем равен 12 часов, но он может укорачиваться или удлиняться в зависимости от количества употреблённого спирта.
Какие симптомы отравления?
- Первый период (начальный) проявляется всего несколько часов, не более 12, и характеризуется лёгким опьянением. Человека беспокоит незначительная слабость и невнятная речь, но в целом самочувствие нормальное. В это время на отравление этиленгликолем указывает только необычный сладковатый запах, исходящий от человека. В редких случаях беспокоит тошнота, периодическая рвота, боли в животе.
- Спустя 12 часов после периода мнимого благополучия, возникает головокружение, головные боли, жажда и тошнота.
- К симптомам отравления этиленгликолем в это время относятся рвота, сильнейшие боли в желудке, которые напоминают признаки острого живота, боль в пояснице и мышцах.
- Немного позже на первое место выходят признаки поражения нервной системы: возбуждение и потеря сознания, появляются многочисленные судороги, увеличивается температура тела.
- Отравление этиленгликолем проявляется ещё и нарушением работы сердца и сосудов: увеличивается частота биения, снижается артериальное давление.
- Нарушается работа дыхательной системы: постепенно появляется одышка, поверхностное дыхание и отёк лёгких.
- Тяжёлые больные теряют сознание.
- Приблизительно на пятые сутки развивается нарушение в работе почек и печени. Из-за почечной недостаточности летальный исход наблюдается в течение одной недели.
- Смерть наступает в первые дни острого отравления из-за паралича дыхательного центра, отёка лёгких и вследствие сердечно-сосудистой недостаточности.
Лёгкое отравление этиленгликолем наблюдается чаще при вдыхании его паров небольшой концентрации. Оно проявляется незначительными симптомами: слабостью, подташниванием, головокружением.
Первая помощь при отравлении
К сожалению, часто причиной запоздалой или несвоевременной помощи становится лёгкое течение отравления, хроническая интоксикация парами этого спирта или позднее обращение пострадавшего человека к медработникам. В этом случае продукты распада гликоля уже оказывают своё повреждающее действие на внутренние органы и наносят непоправимый ущерб здоровью.

этанол — антидот при отравлении этиленгликолем
Что можно сделать на доврачебном этапе, чтобы помочь пострадавшему? Для этого необходимо быть уверенным в употреблении именно этого вещества. Если этиленгликоль был выпит недавно — нужно незамедлительно промыть желудок и ввести слабительное. Активированный уголь не окажет выраженного эффекта.
Быстро помочь при отравлении этиленгликолем, может, антидот — этанол. В этом случае применяется во внутрь его 30%-й раствор или 5%-й вводится внутривенно. А также в качестве антидота используется кальция хлорид или глюконат 10%-й раствор внутривенно или внутрь.
Не у всех под рукой могут оказаться нужные лекарства для оказания экстренных мероприятий. В этом случае неотложная помощь при отравлении этиленгликолем заключается во введении через зонд или рот обычной водки.
Если человек без сознания — его нужно уложить набок и дать доступ кислорода — открыть окно, развязать галстук и освободить от стягивающей одежды.
До момента начала активных действий нужно вызвать бригаду скорой помощи, так как пострадавшему понадобится госпитализация.
При отравлении этиленгликолем у детей нужно действовать незамедлительно и как можно скорее доставить пострадавшего малыша в ближайшую больницу!
Лечение отравления в стационаре
После госпитализации больному человеку проводят курс интенсивной терапии. Если пострадавшему не был дан антидот бригадой скорой помощи, то по прибытии в стационар его вводят сразу же.
Дальше лечение заключается в применении симптоматических препаратов для коррекции работы жизненно важных органов и систем.
- При отравлении этиленгликолем пострадавшему обеспечивают физический покой, доступ кислорода.
- Назначают витамины группы B и C, АТФ (аденозинтрифосфорная кислота).
- При необходимости вводят преднизолон.
- При отравлении этиленгликолем назначают в большом количестве фолиевую кислоту, чтобы связать продукты распада этого двухатомного спирта.
- Вводят солевые растворы.
Профилактика отравления
Какая должна быть профилактика отравления этиленгликолем?
- При работе с химическими веществами, содержащими этиленгликоль, нужно использовать индивидуальные средства защиты.
- Не стоит пить подозрительные жидкости.
- Хранить в недоступном для детей месте все химикаты для защиты и обработки машины, а также уборки помещений.
Этиленгликоль — насколько опасно это соединение? Нельзя недооценивать его негативное влияние на организм человека. Симптомы отравления, при попадании спирта внутрь, развиваются практически молниеносно, а смерть может наступить, спустя всего 5 дней. Отравление этиленгликолем очень легко предупредить и вылечить, если известно, что человек выпил. В противном случае терапия затягивается надолго.
Жидкий теплоноситель на основе этиленгликоля
Водные растворы на основе этиленгликоля широко используются в системах теплопередачи, где температура теплоносителя может быть ниже 32 o F (0 o C) . Этиленгликоль также обычно используется в системах отопления, которые временно не могут работать (в холодном состоянии) в среде с морозными условиями, например, в автомобилях и машинах с двигателями с водяным охлаждением.
Этиленгликоль - наиболее распространенная антифризная жидкость для стандартных систем отопления и охлаждения.Следует избегать использования этиленгликоля, если есть малейшая вероятность утечки в питьевую воду или системы обработки пищевых продуктов. Вместо этого обычно используются растворы на основе пропиленгликоля.
Удельная теплоемкость, вязкость и удельный вес раствора воды и этиленгликоля значительно зависят от процентного содержания этиленгликоля и температуры жидкости. Свойства настолько сильно отличаются от чистой воды, что системы теплопередачи с этиленгликолем должны быть тщательно рассчитаны для реальной температуры и раствора.
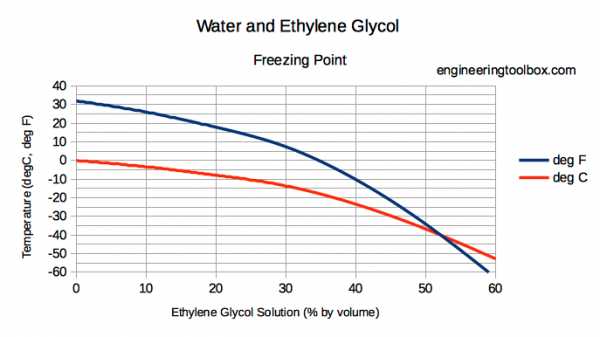
Точка замерзания водных растворов на основе этиленгликоля
Точки замерзания водных растворов на основе этиленгликоля при различных температурах указаны ниже
| Точка замерзания | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Раствор этиленгликоля (% по объему ) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 90 | 100 | |
| Температура | ( o F) | 32 | 25.9 | 17,8 | 7,3 | -10,3 | -34,2 | -63 | ≈ -51 | ≈ -22 | 9 |
| ( o C) | 0 | - 3,4 | -7,9 | -13,7 | -23,5 | -36,8 | -52,8 | ≈ -46 | ≈ -30 | -12,8 | |
Этиленгликоль и вода из-за возможного образования слякоти растворы не следует использовать в условиях, близких к точкам замерзания.
Динамическая вязкость водных растворов на основе этиленгликоля
Динамическая вязкость - μ - водных растворов на основе этиленгликоля при различных температурах указаны ниже
| Динамическая вязкость - μ - ( сантипуаз) | ||||||||
|---|---|---|---|---|---|---|---|---|
| Температура | Раствор этиленгликоля (% по объему) | |||||||
| ( o F) | ( o C) | 25 | 30 | 4050 | 60 | 65 | 100 | |
| 0 | -17.8 | 1) | 1) | 15 | 22 | 35 | 45 | 310 |
| 40 | 4,4 | 3 | 3,5 | 4,8 | 6,5 | 9 | 10,2 | 48 |
| 80 | 26,7 | 1,5 | 1,7 | 2,2 | 2,8 | 3,8 | 4,5 | 15,5 |
| 120 | 48.9 | 0,9 | 1 | 1,3 | 1,5 | 2 | 2,4 | 7 |
| 160 | 71,1 | 0,65 | 0,7 | 0,8 | 0,95 | 1,3 | 1,5 | 3,8 |
| 200 | 93,3 | 0,48 | 0,5 | 0,6 | 0,7 | 0,88 | 0,98 | 2,4 |
| 240 | 115.6 | 2) | 2) | 2) | 2) | 2) | 2) | 1,8 |
| 280 | 137,8 | 900 2)2) | 2) | 2) | 2) | 2) | 1.2 | |
- ниже точки замерзания точка
Примечание! Динамическая вязкость водного раствора на основе этиленгликоля увеличивается по сравнению с динамической вязкостью чистой воды.Как следствие, потеря напора (потеря давления) в системе трубопроводов с этиленгликолем на увеличена на по сравнению с чистой водой.
Удельный вес водных растворов на основе этиленгликоля
Удельный вес - SG - водных растворов на основе этиленгликоля при различных температурах указан ниже
| Удельный вес - SG - | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Температура | Раствор этиленгликоля (% по объему) | ||||||||||
| ( o F) | ( o C) | 25 | 30 | 40 | 50 | 60 | 65 | 100 | |||
| -40 | -40 | 1) | 1) | 1) | 1) | 1.12 | 1,13 | 1) | |||
| 0 | -17,8 | 1) | 1) | 1,08 | 1,10 | 1,11 | 1,12 | 1,16 | |||
| 40 | 4,4 | 1,048 | 1,057 | 1,07 | 1,088 | 1,1 | 1,11 | 1,145 | |||
| 80 | 26,7 | 1.04 | 1.048 | 1.06 | 1.077 | 1.09 | 1.095 | 1,13 | |||
| 120 | 48.9 | 1.03 | 1.038 | 1.05 | 1.064 | 1.077 | 1.082 | 1.115 | 1.077 | 1.082 | 1.115 900 |
| 160 | 71,1 | 1,018 | 1,025 | 1,038 | 1,05 | 1,062 | 1,068 | 1,1 | |||
| 200 | 93.3 | 1.005 | 1.013 | 1.026 | 1.038 | 1.049 | 1.054 | 1.084 | |||
| 240 | 115,6 | 2) | 2) | 54 2) 2) | 2) | 2) | 1.067 | ||||
| 280 | 137,8 | 2) | 2) | 2) | 2) | 2) | 2) | 1.05 | |||
- ниже точки замерзания
- выше точки кипения
Примечание! Удельный вес водных растворов на основе этиленгликоля увеличен по сравнению с удельным весом чистой воды.
Плотность водных растворов на основе этиленгликоля
Поверните экран, чтобы увидеть всю таблицу.
Пример - Объем расширения в системе отопления с этиленгликолем
Система отопления с объемом жидкости 0.8 м 3 защищен от замерзания 50% (по массе, массовая доля 0,5) этиленгликоль. Температура установки системы составляет 0 o C , а максимальная рабочая температура среды составляет 80 o C .
Из приведенной выше таблицы видно, что плотность раствора при температуре установки может достигать 1090 кг / м 3 - а средняя плотность при рабочей температуре может составлять всего 1042 кг / м 3 .
Массу жидкости при установке можно рассчитать как
м inst = ρ inst V inst (1)
= (1090 кг / м 3 ) (0,8 м 3 )
= 872 кг
где
м inst = масса жидкости при установке (кг)
ρ inst = плотность при установке (кг / м 3 )
V inst = объем жидкости при установке (м 3 )
Масса жидкости в системе во время работы будет такой же, как масса в системе во время установки
м inst = м op (2)
= ρ op V op 9002 6
где
м op = масса жидкости при работе (кг)
ρ op = плотность при работе (кг / м 3 )
Vop = объем жидкости при работе (м 3 )
(2) можно изменить для расчета рабочего объема жидкости как
V op = м inst / ρ op (2b)
= (872 кг) / ( 1042 кг / м 3 )
= 0.837 м 3
Требуемый объем расширения, чтобы избежать давления, можно рассчитать как
ΔV = V op - V inst (3)
= (0,837 м 3 ) - (0,8 м 3 )
= 0,037 м 3
= 37 литров
где
ΔV = объем расширения (м 69 64) Объем расширения можно рассчитать как ΔV = ( ρ inst / ρ op - 1 ) V inst26 4 (4) 900 Теплота водных растворов на основе этиленгликоля Удельная теплоемкость - c p - водных растворов на основе этиленгликоля при различных t температуры указаны ниже Поверните экран на всю таблицу. Примечание! Удельная теплоемкость водных растворов на основе этиленгликоля на меньше на , чем удельная теплоемкость чистой воды. Для системы теплопередачи с этиленгликолем циркулирующий объем должен быть увеличен на по сравнению с системой только с водой. В растворе 50% с рабочими температурами выше 36 o F удельная теплоемкость уменьшается примерно на 20% . Сниженную теплоемкость необходимо компенсировать за счет циркуляции большего количества жидкости. Примечание! Плотность этиленгликоля выше, чем у воды - проверьте приведенную выше таблицу удельного веса (SG), чтобы снизить чистое воздействие на теплопередающую способность. Пример - удельная теплоемкость водного раствора этиленгликоля 50% / 50% равна 0.815 при 80 o F (26,7 o C). Удельный вес при тех же условиях составляет 1,077. Чистое воздействие можно оценить как 0,815 * 1,077 = 0,877. Автомобильные антифризы не следует использовать в системах отопления, вентиляции и кондиционирования воздуха, поскольку они содержат силикаты, которые могут вызвать загрязнение. Силикаты в автомобильных антифризах используются для защиты алюминиевых деталей двигателя. Примечание! Для растворов этиленгликоля следует использовать дистиллированную или деионизированную воду. Городскую воду можно обрабатывать хлором, который вызывает коррозию. Не следует использовать системы автоматической подпитки, поскольку утечка может загрязнить окружающую среду и ослабить защиту системы от замерзания. Для полной таблицы с точками кипения - поверните экран! Увеличение циркулирующего потока для 50% растворов этиленгликоля по сравнению с чистой водой указаны в таблице ниже Коррекция перепада давления и комбинированная поправка перепада давления и увеличения расхода для 50% раствора этиленгликоля по сравнению с чистой водой указаны в таблице ниже Поставщик медицинских услуг будет измерять и контролировать жизненно важные показатели человека, включая температуру, пульс, частоту дыхания и артериальное давление. Диагностика токсичности этиленгликоля обычно проводится с помощью комбинации анализов крови, мочи и других анализов, таких как: Анализы покажут повышенный уровень этиленгликоля, химические нарушения в крови и возможные признаки почечной недостаточности, а также повреждения мышц или печени. Большинство людей с отравлением этиленгликолем нуждаются в госпитализации в отделение интенсивной терапии (ОИТ) для тщательного наблюдения. Может потребоваться дыхательный аппарат (респиратор). Тем, кто недавно (в течение 30–60 минут после обращения в отделение неотложной помощи) проглотил этиленгликоль, может быть произведена откачка желудка (отсасывание). Это может помочь удалить часть яда. Другие виды лечения могут включать: В тяжелых случаях можно использовать диализ (аппарат почек) для прямого удаления этиленгликоля и других ядовитых веществ из крови.Диализ сокращает время, необходимое организму для удаления токсинов. Диализ также необходим людям, у которых в результате отравления развивается тяжелая почечная недостаточность. Он может понадобиться в течение многих месяцев, а возможно, и лет после этого. , Джош Фаркас (вернуться к содержанию) механизм токсичности метанола: Механизм токсичности этиленгликоля: (вернуться к содержанию) (вернуться к содержанию) Ниже приведены типичные симптомы, когда они проглатываются отдельно.При одновременном приеме внутрь с этанолом начало токсичности может быть отложено. (вернуться к содержанию) (вернуться к содержанию) Осмоляльный промежуток традиционно использовался в качестве скринингового теста на употребление токсичного алкоголя. Однако в этой главе утверждается, что от нее следует отказаться. Это немного спорный, но есть значительное количество доказательств того, что osmolal разрыв не приносит никакой пользы.Более того, многие токсикологи говорят об этом уже давно. Причины прекращения измерения осмоляльного зазора следующие: (вернуться к содержанию) Со временем осмолярная щель уменьшается, а анионная щель увеличивается.Это может сделать анионный зазор более полезным, чем осмолярный зазор. Анионная щель может быть поразительно высокой. (вернуться к содержанию) Прекрасный недавний пример: тормозная жидкость. Устойчивый «высокий уровень лактата», несмотря на устранение ацидоза. pic.twitter.com/ts3ddv87Rs - Виктория Стивен (@EMcardiac) 14 марта 2018 г. (назад к содержанию) В моем лучшем голосе Роберта Дюваля: «Мне нравится запах кристаллов оксалата кальция в отделении интенсивной терапии. - Джоэл Топф, MD FACP (@kidney_boy) 15 октября 2019 г. (назад к содержанию) (вернуться к содержанию) (к содержанию) (вернуться к содержанию) (вернуться к содержанию) (вернуться к содержанию) Они могут способствовать метаболизму токсичных побочных продуктов кислоты. Или они могут безвредно выделяться с мочой. (вернуться к содержанию) (вернуться к содержанию) (назад к содержанию) (вернуться к содержанию) Чтобы эта страница оставалась небольшой и быстрой, вопросы и обсуждение этого сообщения можно найти на другой странице. здесь . Цао XL, Чжу Дж. [2001]. Метод контроля содержания глимов в воздухе и его применение для измерения выбросов выхлопных газов. Chemosphere 45 (6-7): 911-917. NIOSH [1996]. NMAM 5523, выпуск 1: Гликоли. В кн .: Руководство по аналитическим методам НИОШ. 4-е изд. Цинциннати, Огайо: У.S. Департамент здравоохранения и социальных служб, Служба общественного здравоохранения, Центры по контролю и профилактике заболеваний, Национальный институт охраны труда и здоровья, Публикация DHHS (NIOSH) № 94-113. Пендерграсс С.М. [1999]. Определение гликолей в воздухе: разработка методологии отбора проб и анализа и применение к театральным дымам. Am Ind Hyg Assoc J 60: 452-457. Поттер В. [1999]. Этиленгликоль Метод PV2024. OSHA Солт-Лейк-Сити, штат Юта: Министерство труда США, Технический центр OSHA в Солт-Лейк-Сити, Группа хроматографии. Kenyon AS, Shi X, Wang Y, Ng WH, Prestridge R, Sharp K [1998]. Простое обнаружение примесей диэтиленгликоля / этиленгликоля в глицерине и сырье на основе глицерина на месте с помощью тонкослойной хроматографии. J AOAC Int 81 (1): 44-50. Маурер Х. Х., Петерс Ф. Т., Пол Л. Д., Кремер Т. [2001]. Утвержденный газовый хроматографо-масс-спектрометрический анализ для определения антифризов этиленгликоля и диэтиленгликоля в плазме крови человека после пивалилирования с помощью микроволнового излучения. J Chromatogr B: Biomed Appl 754 (2): 401-409. Нильссон Л., Джонс А.В. [1992]. 2,3-Бутандиол: вещество, потенциально мешающее при анализе этиленгликоля ферментативным методом. Clin Chim Acta 208 (3): 225-229. Oudhoff KA, Schoenmakers PJ, Kok W.T. [2003].Характеристика полиэтиленгликолей и полипропиленгликолей методами капиллярного зонного электрофореза и мицеллярной электрокинетической хроматографии. J Chromatogr A 985 (1-2): 479-491. Шимански А., Вырвас Б., Шимановска М., Лукашевский З. [2001]. Определение короткоцепочечных полиэтиленгликолей и этиленгликоля в пробах окружающей среды. Water Res 35 (15): 3599-3604. Валь А., Азаруаль Н., Имбенотт М., Матье Д., Форзи Дж., Картиньи Б., Вермеерш Дж., Лермитт М. [1998]. Отравление метанолом и этиленгликолем: спектроскопия ЯМР 1H как эффективный клинический инструмент для диагностики и количественной оценки.Токсикология 128 (1): 73-81.
Точки кипения Растворы этиленгликоля
Температура кипения Раствор этиленгликоля
(% по объему) 0 10 20 30 40 50 60 70 80 90 100 Температура ( o F) 212 214 216 220 220 225 232 245 260 288 386 ( o C) 100 101.1 102,2 104,4 104,4 107,2 111,1 118 127 142 197 Требуется увеличение расхода для раствора 50% этиленгликоля
Температура жидкости Увеличение расхода
(%) ( o F) ( o C) 40 4.4 22 100 37,8 16 140 60,0 15 180 82,2 14 220 104,4 14 Коррекция перепада давления и комбинированная поправка перепада давления и объемного расхода для 50% раствора этиленгликоля
. Температура жидкости Коррекция падения давления при равных скоростях потока
(%) Комбинированная коррекция перепада давления и расхода
(%) ( o F) ( o C) 4 0 4.4 45 114 100 37,8 10 49 140 60,0 0 32 180 82,2 -6 23 220 104,4 -10 18 Отравление этиленгликолем: Медицинская энциклопедия MedlinePlus
Отравление этиленгликолем и метанолом
Вы здесь: Home / IBCC / Отравление этиленгликолем и метанолом
СОДЕРЖАНИЕ
биохимия
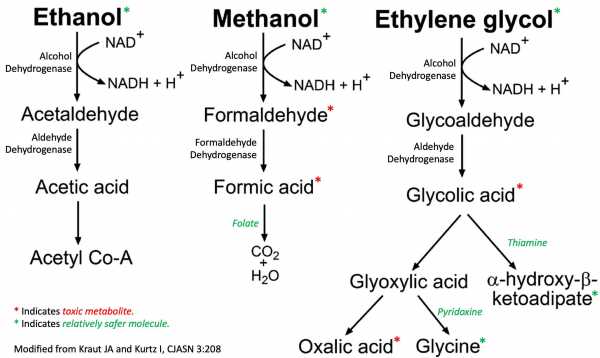
эпидемиология
общие сценарии
этиленгликоль находится в:
метанол находится в:
симптомы
этиленгликоль
метанол
лабораторная панель
лабораторий для получения
осмолярный зазор
теоретическая проблема №1: без стандартизации
теоретическая проблема # 2: низкая чувствительность
теоретическая проблема № 3: низкая специфичность
Итог: плохие результаты теста
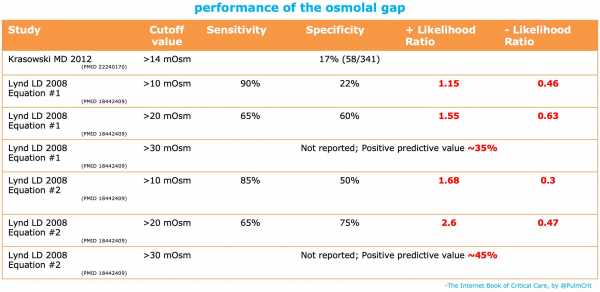
анионный разрыв
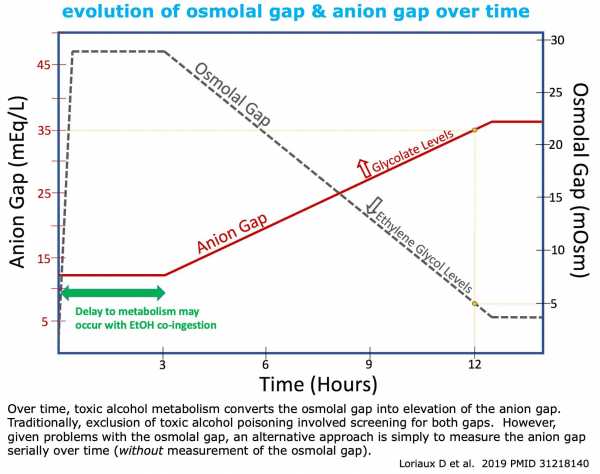
чувствительность

специфичность
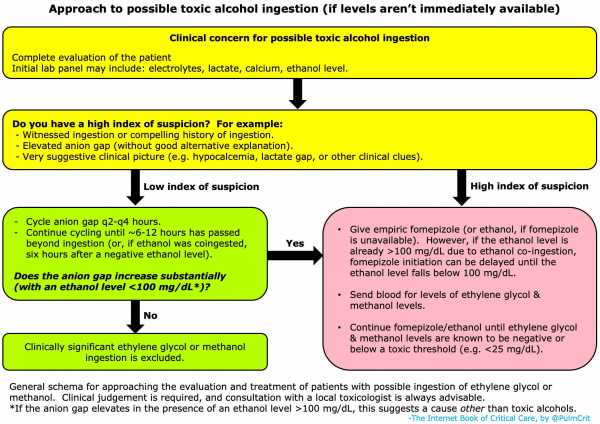
лактатный зазор
реальный уровень лактата
Артефактное повышение «лактата» и «лактатной щели»
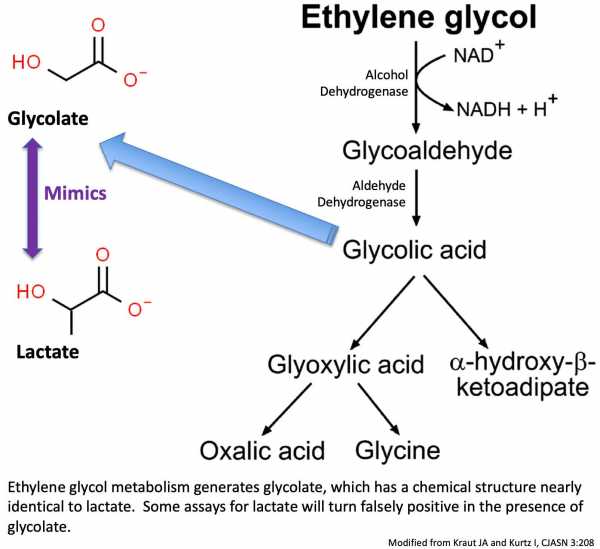
другие лабораторные свидетельства токсичности этиленгликоля
гипокальциемия
кристаллы оксалата кальция
Пахнет… диализом »pic.twitter.com/3ZeGxGwOFx
специальные тесты для метанола или этиленгликоля
прямые измерения этиленгликоля или метанола
Традиционный анализ с использованием газовой хроматографии
Ветеринарный анализ метаболитов этиленгликоля
дезактивация
дезактивация
Блокада алкогольдегидрогеназы
Возможные показания к началу блокады алкогольдегидрогеназы
когда прекратить блокаду алкогольдегидрогеназы
фомепизол (он же 4-метилпиразол)
этанол
гемодиализ
ролей гемодиализа
Показания к диализу
продолжить блокаду алкогольдегидрогеназы во время диализа
прочие технические данные
жидкости и электролиты
бикарбонат для лечения ацидоза
гипокальциемия
витамины
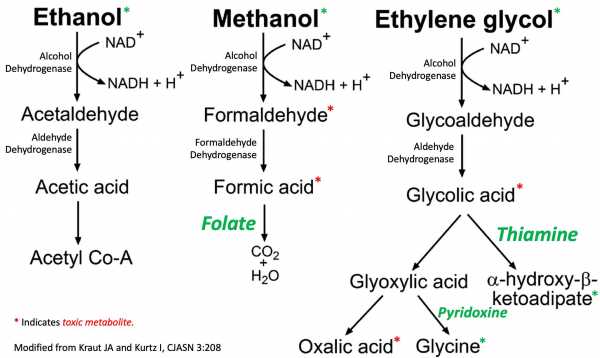 для этиленгликоля:
для этиленгликоля:
для метанола:
Смерть мозга, вызванная метанолом
сводка
лабораторий, чтобы получить

подкаст

Следуйте за нами в iTunes
вопросы и обсуждения
Далее:
Интернет-книга интенсивной терапии - это онлайн-учебник, написанный Джошем Фаркасом (@PulmCrit), доцентом кафедры легочной медицины и реанимации Университета Вермонта.
. CDC - База данных по безопасности и охране здоровья при чрезвычайных ситуациях: Системный агент: ЭТИЛЕНГЛИКОЛЬ
AIR MATRIX
Bost RO, Sunshine I [1980]. Анализ этиленгликоля методом газовой хроматографии. J. Anal Toxicol 4 (2): 102-103.
Хоуз? P, Chaussard J [1993]. Одновременное определение этиленгликоля, пропиленгликоля, 1,3-бутиленгликоля и 2,3-бутиленгликоля в сыворотке крови человека и моче методом газовой хроматографии на колонке с широким отверстием. J Chromatogr B: Biomed Appl 619 (2): 251-257.











